濃度は、割合を100倍した百分率 (%)で表されている ので、 割合を求めるには濃度を100で割る必要がある のです。 この問題では濃度が8%なので、 割合は8を100で割った008 になりま中1で学習する「質量パーセント濃度」についての計算問題集です。 PDFファイルの販売になります。 中学1年生以上向けの内容になっています。 中学3年生の復習教材としても使用できます。 収録内容 問題番号1 質量パーセント濃度を求める問題 質量パーセント濃度から溶質の量を求める水素イオン濃度を求められないとpH計算ができません。 水酸化物イオン濃度も同様です。 そこで、pHの求め方は知っていても水素イオン濃度が求められないという場合があるといけないので、計算問題をいくつかやっておきましょう。 続きを読む
配制溶液浓度计算公式 西瓜视频搜索
濃度 計算 問題集
濃度 計算 問題集-質量パーセント濃度 計算問題 質量パーセント濃度 計算問題 次の問いに答えよ。 (1) 砂糖水250gがある。この中に砂糖がg溶けている場合、この砂糖水の質量パーセント濃度は何%か。 (2) 0gの水に、砂糖を50g溶かした。 このときできた砂糖水は何gか。問題9 点滴で水分を1日に1500ml補給する患者がいます。 1時間に何ml入るようにセットすればいいですか。 計算では1の位を四捨五入してください。 問題10 成人は体重1kgあたり50mlの水分が必要です。 体重48kgの点滴を女性の患者では




1 4觀念09溶液的稀釋與混合 Youtube
化学計算問題 NISHIMURA Yoshikazu 5 濃度②(溶液の希釈,%→mol/L の換算) ★★★ 問題 98 %の濃硫酸(密度18 g/cm3)を水で希釈し,24 mol/L の希硫酸(密度114 g/cm3)を300 mL 作りたい。 (1) この濃硫酸のモル濃度は何mol/L か。質量パーセント濃度を求める式の 途中に空欄をあけて、 「溶質」「溶媒」「溶液」という 言葉をそこに入れさせる、 という問題も出ますよ。 そういう問題で得点するためにも、 上記ページをよく読んでくださいね! 濃度の計算は、 "具体的なもの質量パーセント濃度 計算問題 次の問いに答えよ。 (1) 砂糖水250gがある。この中に砂糖がg溶けている場合、この砂糖水の質量パーセント濃度は何%か。 (2) 0gの水に、砂糖を50g溶かした。 このときできた砂糖水は何gか。
すると、 滴定によって未知の濃度などを求めることが不可能になってしまいます 。 このような場合も存在するので、頭に入れておきましょう。 中和滴定の計算問題 では実際に計算問題の解き方と練習問題を見ていきましょう。 spi試験で出題される濃度算は、水に溶けている食塩の量を計算したり、水の量を変化させたときの濃度を計算したりする問題です。割合(% パーセント)を考える必要があり、問題が複雑になりやすい分野です。 問題のタイプとしては、以下の3つがあります。 では早速「濃度算」の問題にチャレンジしてみましょう。 濃度の問題: 問題 1: 14%の食塩水と、24%の食塩水を混ぜ合わせて%の食塩水を800 gつくるには14%の食塩水は何g混ぜればよいか。 A 1 g B 160 g C 180 g D 240 g E 3 g F 360 g G 400 g H AからGに
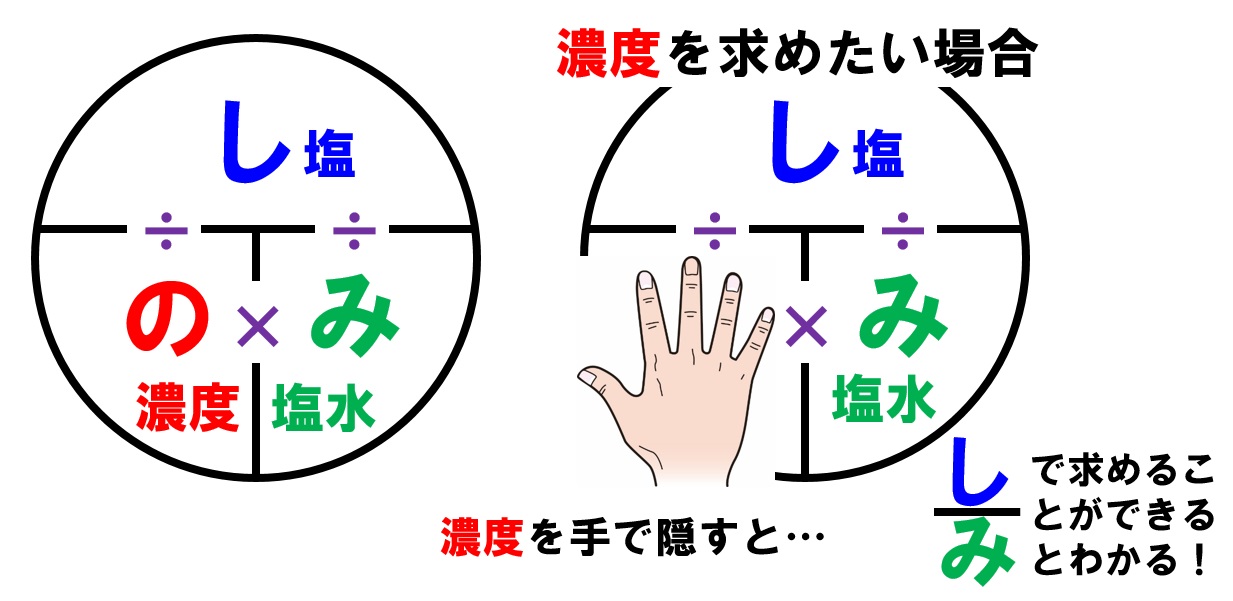
含まれる食塩 (g) = 食塩水 (g) × 濃度 (%) 100濃度のわからない食塩水MとNがそれぞれ800gずつある。 Mから300gとNから500gを取り出してこれらを混ぜると8%の食塩水になり、残りの食塩水をすべて混ぜてさらに、水を160g加えると10%の食塩水ができる。 MとNの濃度をそれぞれ求めなさい。 式 答濃度の計算 「溶液=溶質+溶媒」を思い出そう! 小中学校で、食塩水の濃度を求める計算問題を解いた記憶があると思います。"食 塩水(溶液)は、食塩(溶質)が水(溶媒)に溶けているもの"、ということを思い 出しましょう。



粉笔网




質量パーセント濃度の計算問題集 応用編 Menon Network
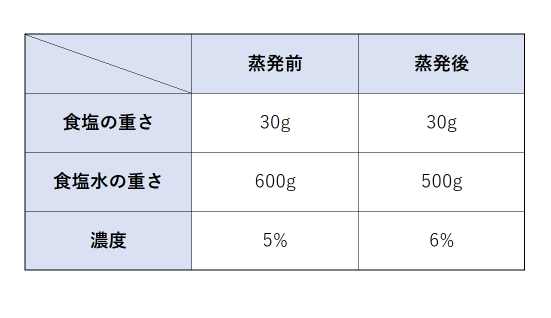
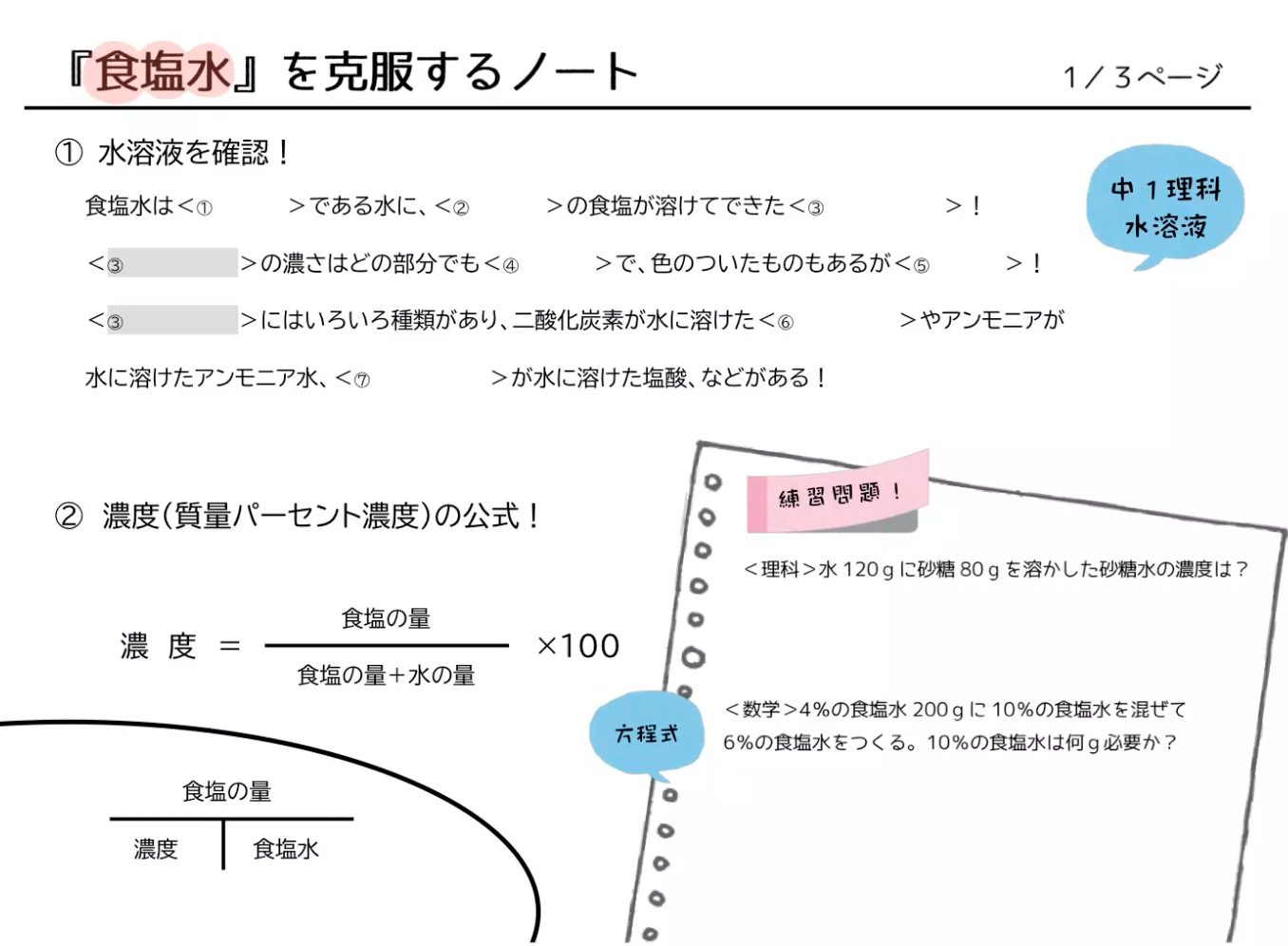
「濃度」を計算するためには、「食塩の重さ」を「食塩水の重さ」で割って求めます。 そして「濃度」は百分率 (%)で表しますから、100をかけることになります。 つまり公式2は、「濃度 (%)」=「食塩の重さ」÷「食塩水の重さ」×100まずは、問題文の内容を読み取っていきます。 この問題では、質量パーセント濃度が 8% 、密度が 11g/mL の水酸化ナトリウム水溶液があります。 この水溶液の モル濃度 を求めるのですね。 これまでの問題と同じ形式なので、解くための流れを押さえましょう。12. 食塩15gと水285gを混ぜ、火にかけていきました。 (1)すべて混ざり合うと濃さは何%ですか。 (2)火をかけ続け、水が何gか蒸発したので、濃さを調べたところ、10%でした。




5种计算溶液浓度的简便方法 百科全书 21




高考化学总复习专题一 化学常用计量及其应用 知乎
物質 問題 チェックテスト いろいろな物質 密度計算 水溶液 濃度溶解度計算 気体 状態変化 基本問題 いろいろな物質 密度計算問題 身の回りの物質 気体1 気体2 気体3 水溶液の性質 水溶液の性質2 濃度計算問題 アンモニアの噴水実験 メスシリンダーの使いモル濃度は 13 で学んだ通り、モル濃度( mol / L )= 溶質の物質量( mol )÷ 溶液の体積( L )で導きます。 また溶液の体積は、次のように変換することもできることも使って計算しましょう。 溶液の体積( L )= 溶液の体積( mL )÷ 1000 中学1年理科。質量パーセント濃度の計算特訓を行います。 レベル★★★☆ 重要度★★☆☆ ポイント:食塩(溶質)の量に注目問題のダウンロードはこちら!計算プリント「濃度計算特訓」質量パーセント濃度の計算質量パーセント濃度の計算を行う前に



速解丨數量關係中的濃度問題 雪花新闻




3种方法来计算溶液浓度
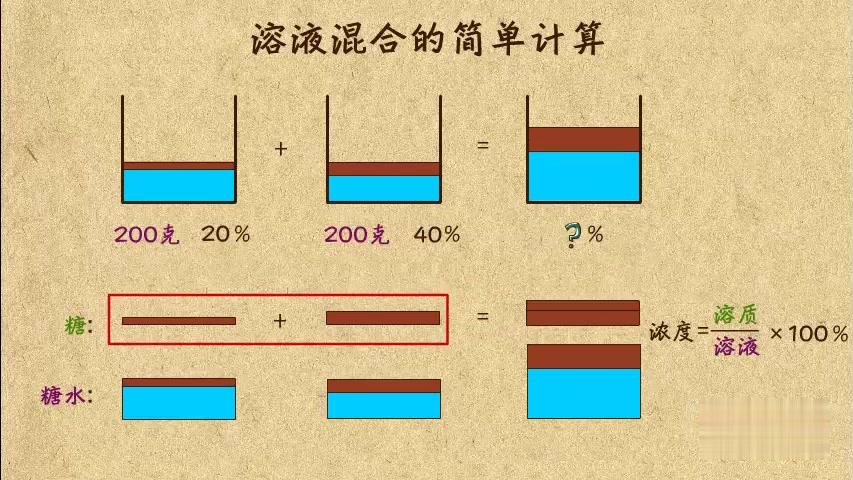
濃度の違う食塩水を混ぜる問題の解き方1計算問題付 それでは、濃度算に関する練習問題を解いていきましょう。 ・例題1 濃度が5%の食塩水0gと、濃度が10%の食塩水300gを混ぜた際の濃度は何パーセントになるでしょうか。 ・解答1物質 問題 チェックテスト いろいろな物質 密度計算 水溶液 濃度溶解度計算 気体 状態変化 基本問題 いろいろな物質 密度計算問題 身の回りの物質 気体1 気体2 気体3 水溶液の性質 水溶液の性質2 濃度計算問題 アンモニアの噴水実験 メスシリンダーの使い<練習問題> 濃度%の食塩水に50gの食塩を入れ、100gの水を蒸発させたところ、 40%の食塩水になった。最初にあった食塩水は何gであったか。 1.300g 2.350g 3.400g 4.450g 5.500g <解




中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu




小学数学浓度问题 抓住两个量 就没有难度了 Tnaot
第Ⅱ章 栄養士のための割合を使った計算問題 第Ⅰ章で、割合計算の基礎を学んできましたが、割合の基礎が分かれば、栄養士に必要な計 算問題は、少しの応用でできるようになります。 第1節 三大栄養素に関する計算問題 例題1物質の濃度について、練習問題を解いていきましょう。 質量パーセント濃度〔%〕= (溶質の質量〔g〕/溶液の質量〔g〕)×100 (1)は、質量パーセント濃度を求める問題です。水溶液濃度計算に関する問題を解決する際に,生徒 は習熟度別にどのような知識・技能が不足していてつ まずいているのかを明らかにし,水溶液濃度計算にお ける学習指導法を検討する. Ⅲ.方法 1.調査対象と調査時期




小學數學寒假自補 濃度問題口訣及解題方法附經典應用題及答案 每日頭條




小學數學寒假自補 濃度問題口訣及解題方法附經典應用題及答案 每日頭條
演習問題(関数電卓を使用すること) 1.モル濃度(molarity) を計算しなさい,ただし,原子量はH=1, C=12, N=14, O=16, 中学受験でよく出題される食塩水の濃度の問題です。 濃度は割合の考え方が身につけて基本的な問題はすぐに解けるように練習してください。 食塩水と食塩水を混ぜる問題は面積図で考えることが多くなります。 また比を使う考え方も利用



配制溶液浓度计算公式 西瓜视频搜索




質量パーセント濃度の計算問題集 応用編 Menon Network




预初 六年级 数学浓度问题解析 数学浓度问题的计算公式 上海爱智康



被绕晕在溶液稀释计算中 送你一个溶液稀释计算神器 话题 科研狗社区




質量パーセント濃度の計算問題集 基本編 Menon Network




4种计算摩尔浓度的方法 提示 21




1x版九年级化学下册第九单元溶液9 3溶液的浓度教案新人教版下载 Word模板 爱问共享资料



小学奥数 浓度问题下载 Word模板 爱问共享资料




国考行测数量关系指导之用 溶质 突破浓度问题 哔哩哔哩



1 4觀念10溶液的濃度換算 Youtube




小學數學寒假自補 濃度問題口訣及解題方法附經典應用題及答案 每日頭條




Swf Ishare Down Sina Com Cn Agkvy8cnh5n Jpg Ssi



求助 关于营养液山崎配方中浓度计算问题 农林 小木虫 学术科研互动社区




用例子理解排列组合及基本公式如何计算 搜狗指南




モノマナビ研究所




中1理科 濃度の計算 映像授業のtry It トライイット



预初 六年级 数学浓度问题解析 数学浓度问题的计算公式 上海爱智康



摩尔浓度计算 西瓜视频搜索




中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu



数量关系 核心方法 线段法 知乎




盐水混合浓度计算公式 西瓜视频




浓度问题 知乎




食塩水問題 濃度算 の2つの解き方とポイントを図で解説 数学fun




小学数学浓度问题 抓住两个量 就没有难度了 Tnaot



小学五年级数学浓度问题知识点讲解 五年级奥数题 奥数网



腾讯视频



物质的量浓度2 2 备课吧




透析溶液的浓度计算下载 Word模板 爱问共享资料



溶液加水稀释浓度计算 西瓜视频搜索



氯化钠溶液在生产 生活中都有广泛的用途 现配置1 L 0 2 Mol L Nacl溶液 请回答问题 高中一年级 化学试题 配制一定物质的量浓度 的溶液考点 好技网




Spi3 問題無料 言語非言語テストセンターwebテスト就職一般常識濃度計算 安卓下載 安卓版apk 免費下載



1




高校化学基礎 モル濃度の計算 練習編 映像授業のtry It トライイット




浓度问题 知乎




浓度 知乎



中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu




小升初數學 濃度問題訓練及答案 每日頭條




1 4觀念09溶液的稀釋與混合 Youtube




國一上三段段衝精選類46 濃度問題asepx凱爺數學 Youtube



公考行測秒殺技巧 濃度問題解題方法 愛經驗



行测80分必备 数学运算经典题型全集下载 Word模板 爱问共享资料



硫酸摩尔浓度对照表关于标定硫酸摩尔浓度的计算公式含义的问题 尚书坊



浓度计算公式有哪些 高三网




小升初數學 濃度問題訓練及答案 每日頭條



普通化學濃度計算問題 考試板 Dcard




3种方法来计算溶液浓度




物质的量浓度公式大全 物质的量浓度有哪些计算公式 三人行教育网 Www 3rxing Org




改訂版 大学入試 ゼロからはじめる 化学計算問題の解き方 Amazon Com Books



浓度问题视频动画 西瓜视频



浓度的计算公式浓度计算公式数学 麦税尼网



Q Tbn And9gcr38xa5vgb8 Lvcw7xfxsrasgzdizqbebdgmauom0tf2onrxuqv Usqp Cau



食鹽水濃度計算題 數學板 Dcard



1




粉笔网



1




水的浓度的计算 搜狗搜索



濃度計算の公式はどうして成り立つの 食塩水の問題を割合として理解しよう 中学受験ナビ




小學數學寒假自補 濃度問題口訣及解題方法附經典應用題及答案 每日頭條



浓度问题公式 万图壁纸网



速解丨数量关系中的浓度问题 应用




高校化学基礎 濃度の計算 練習編 映像授業のtry It トライイット




小學數學寒假自補 濃度問題口訣及解題方法附經典應用題及答案 每日頭條




14溶液计算 稀释 浓缩问题溶液初中化学 Youtube




濃度與配比問題 每日頭條



浓度问题 在两杯水中加入盐 比较哪一杯盐水的浓度大 网易视频



课时4 物质的量在化学方程式计算中的应用下载 Word模板 爱问共享资料



看護学科の化学講義 16 溶液濃度計算問題演習 Life Chemistry




濃度稀釋計算問題 濃度稀釋計算



如何计算糖与糖水的质量比 三道题帮你解决 浓度问题




濃度算 食塩水問題 の文章問題 計算ドリル 問題集 数学fun



高一化学物质的量浓度的计算 第五题 信息阅读欣赏 信息村 K0w0m Com



中1理科 数学 食塩水の問題を動画でマスター 公式の覚え方と濃度の計算 マナブレイン




稀释的公式 溶液稀释浓度计算公式是什么 三人行教育网 Www 3rxing Org




怎么算出体积摩尔浓度 Molarity 生活百科




1 4觀念03溶液濃度的表示 重量百分濃度 Youtube




小升初數學之求陰影面積問題 濃度問題最全講解 每日頭條




教重量百分濃度計算題 小笨童的理化天地 隨意窩xuite日誌




3种方法来计算溶液浓度




预初 六年级 数学浓度问题解析 数学浓度问题的计算公式 上海爱智康



浓度的计算公式浓度计算公式数学 麦税尼网



浓度的计算公式浓度计算公式数学 麦税尼网




摩尔浓度的计算



高一化学 物质的量浓度稀释问题相关计算 哔哩哔哩 つロ干杯 Bilibili




初中化学质量分数计算问题的八种解题方法 星火网校



配制溶液浓度计算公式 西瓜视频搜索




求溶液的百分浓度公式 溶液百分比浓度的公式 三人行教育网 Www 3rxing Org




日本东电拟排放核污水前不测放射性物质浓度 日网友批 想敷衍了事



如何计算糖与糖水的质量比 三道题帮你解决 浓度问题



配制溶液浓度计算公式 西瓜视频搜索



腾讯视频



数学运算 计算问题之算式计算 91up快学堂




これで分かる モル濃度計算の解き方 大村升次郎 大村升次郎 本 通販 Amazon



一道題目的n種錯法 如果我再把濃度重講一次 你一定懶得聽 在那邊恍神 因為濃度其實你早就懂了 你不 By 有熊老師



公务员 事业单位行测数学如何提高答题速度 这是成功与否的关键 教育资讯 电影风云娱乐网



0 件のコメント:
コメントを投稿